资讯详情
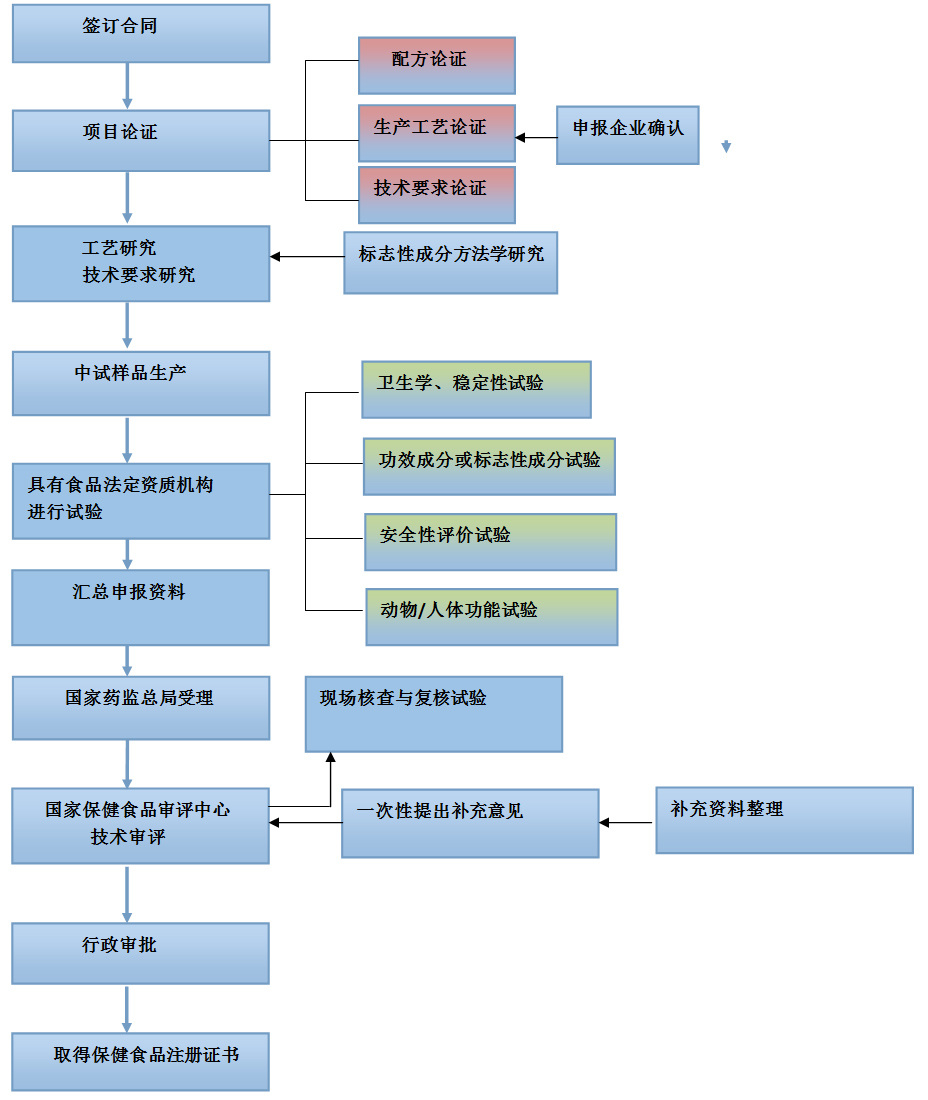
国产保健食品申报流程
发布时间:
2018-03-02 16:38
来源:
针对《保健食品注册与备案管理办法》、《保健食品注册申请服务指南》(2016年版)以及“保健食品含片与颗粒剂指标检测、标志性成分或功效成分检测方法学研究资料、按新版食品安全国家标准修改指标的产品,应提供哪些申报资料”等法规的发布。
结合新法规要求及我公司10多年的保健食品研发注册申报经验,整理保健食品注册申报7个阶段及关键点如下:
第一阶段:前期研究论证
根据贵公司要求,进行配方方案设计,必要情况下召开专家咨询论证会或进行配方功能预实验筛选研究,确定产品最终配方。
1、配方研究论证:原料使用依据合理,符合相关法律法规要求。新法规将重点审评配方配伍及用量与申报功能相关的科学依据。
2、工艺研究论证:根据科学文献查询确定产品工艺,物质基础与工艺相统一。对各工序和使用技术的必要性、科学性和可行性进行充分论证。
3、技术要求研究论证:标志性成分选择应为主要原料含有的性质稳定、能够准确定量、与产品保健功能具有明确相关性的特征成分。理化指标和卫生学等项目符合药典相关剂型要求及GB 16740要求。
第二阶段:工艺研究、技术要求研究
对配方论证、功能实验筛选研究后贵公司确认的配方进行工艺研究,固体剂型主要考察混合均一性、流动性等,液体剂型主要考察辅料使用及口感、工艺灭菌方式。技术要求主要按照审评中心发布“标志性成分或功效成分检测方法学研究资料”应提供哪些研究资料要求进行标志性成分方法学研究。
第三阶段:中试样品生产
在具有保健食品生产资质的企业完成小试工艺研究到中试工艺验证和工艺修正过程。完成三批合格样品生产。含原辅料包材自检、成品按技术要求全项目检测等。
第四阶段:安全性和保健功能试验阶段
将中试样品送到具有法定资质的食品检验机构进行功效成分或标志性成分、卫生学、稳定性试验,安全性评价试验、保健功能(动物、人体)评价试验等。涉及特殊原料应进行品种鉴定、菌种毒力试验。
第五阶段:国家总局受理
国家药监总局对负责保健食品注册申报资料受理工作,并提供产品受理通知书。
第六阶段:技术审评及现场核查
国家药监总局保健食品审评机构负责组织保健食品审评,一次告知补正的全部内容并在3个月内提供补充材料。国家药监总局审核查验机构负责保健食品注册现场核查工作(研发报告、配方、生产工艺及技术要求研究现场、中试加工现场核查)。
第七阶段:国家总局行政审批和制证
国家食品药品监督管理总局对产品进行行政审批和制证。格式“国食健注G+4位年代号+4位顺序号”。
相关附件
在线客服


